Cuando hablamos de vidrio o cristal tratandolos como diferentes resulta complicado saber a lo que nos referimos, en especial en el castellano. En términos no científicos se suelen emplear como sinónimos: ¨Mis ventanas son de vidrio, recién le he comprado cristales nuevos¨ ¿Les resulta conocido?

Casi todo el mundo sabe lo que es una emoción hasta que intenta definirla. En ese momento prácticamente nadie afirma poder. Psicología de la Emoción de 1962
Le haremos comprender que tan diferentes son estos 2 materiales, por lo tanto, continúa leyendo.
¿Qué es Vidrio?
En palabras sencillas, el vidrio es una composición mineral de forma natural o artificial causada por el sometimiento a elevadas temperaturas de 1500 grados centígrados. Su estructura es inorgánica y polimórfica, a partir de compuestos de silicio, sodio y roca caliza. El vidrio no es un compuesto químico sino una mezcla de óxidos.

El vidrio se caracteriza por no contener carbono y polimórfico, ser duro pero frágil a caídas y translúcido. Su estructura base es amorfa, no tiene una forma organizada, como la obsidiana o vidrio volcánico.
Orígenes del vidrio y usos actuales
La historia del vidrio es tan antigua que sus orígenes se pierden en las eras. Por su facilidad de elaboración y su abundancia se llegó a considerar un tipo de roca, sin más valor que para usos decorativos y de bisutería.
En la actualidad, el vidrio es empleado en gran parte de lo que usamos, aunque con la llegada de la era industrial el vidrio fue desplazado por el plástico. En su mayoría, el vidrio se sigue usando en: botellas, gafas, ventanas, etc.
Vidrio industrial en la arquitectura moderna
El vidrio artificial o industrial se elabora principalmente con sílice (arena) boro y fósforo, que al fusionarse alcanzan el estado vítreo que le da el nombre de vidrio.
Al ser tan fáciles de fabricar, económicos y excelentes características son tan cotizados en proyectos arquitectónicos, sobre todo para fachadas de rascacielos.

Los más utilizados en la arquitectura actualmente son:
- Vidrio templado
- Vidrio insulado o DVH (dobles vidriados herméticos)
- Vidrios polarizados UV
- Vidrios de seguridad
- Vidrio laminado
Ahora que estamos entre expertos del vidrio, hablemos un poco acerca de los cristales.
Cristal: El material ordenado ¿Qué es?
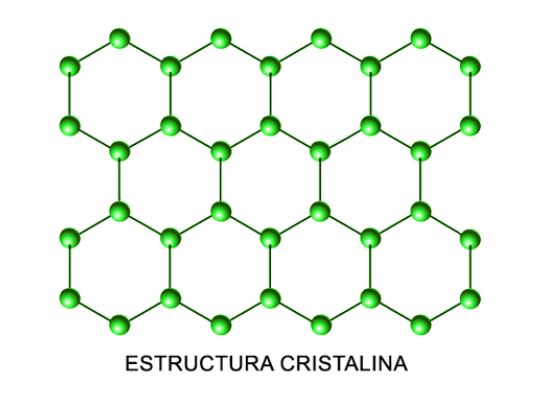
De denomina cristal a un material sólido y homogéneo cuya estructura interna es uniforme. Sus partículas actúan de manera esquemática siguiendo un patrón que se reproduce a lo largo de su forma. Un cristal se produce cuando las partículas existentes en los gases naturales, al ser expuestas a niveles altos de presión y temperatura.

Estas geodas, están condicionadas por la composición de los gases que son las causantes de sus distintivos colores, forma unica y calidad a los cristales.
Usos del cristal en el pasado
El proceso de Verneuil o fusión por llama, fue el único procedimiento que logró de forma eficaz y barata la elaboración de cristales sintéticos.
Gracias a una fabricación rápida, rentable y con mucha demanda, a principios del siglo XIX , se utilizó a para la elaboración de rubíes, zafiros, variedades de corindón. Así como, para las imitaciones de diamantes: rutilo y titanato de estroncio.
Ahora que conocemos las cualidades y atributos de cada uno, sabes…
¿Cuáles son las diferencias entre Vidrio y Cristal?
El cristal se encuentra en la naturaleza en diferentes formas: cuarzos, cristal de roca; mientras que el vidrio es el resultado de un fusión de distintos materiales: Sílice, Sosa y Cal. Sin embargo, existen vidrios creados en la naturaleza, la obsidiana, formado en el interior de los volcanes.
El vidrio de plomo o vidrio óptico es llamado comúnmente ¨cristal¨ por su transparencia tan similar que imita al cristal de roca. Pero, su aspecto no es más que resultado de la implementación de técnicas de refinación y trabajo a materiales más puros. Al momento de su desarrollo se le conoció como falso cristal y era la predilección de los vidrieros por baja cantidad de impurezas y belleza.
Aunque con todo lo mencionado el vidrio pueda ser considerado un tipo de cristal desde el punto de vista científico no lo es. El vidrio carece de consistencia en su estructura, por ello, el vidrio no posee las propiedades moleculares para ser denominado como cristal.
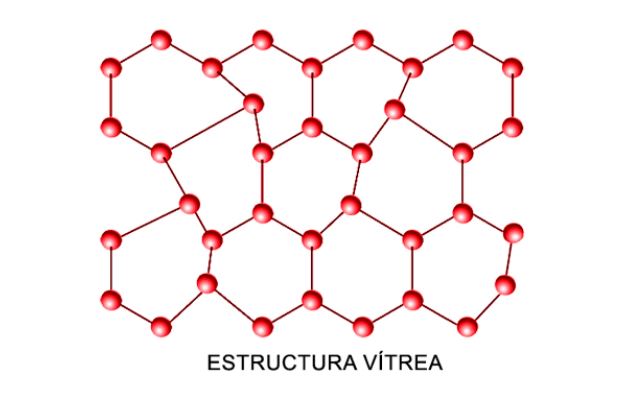
Sin embargo, son esas mismas propiedades amorfas la que permiten que el vidrio sea tan maleable y pueda dársele tantos usos. De hecho, son sus mismas irregularidades estructurales las que permiten que el vidrio sea un material de reciclaje al 100%.
La reutilización del cristal no es factible actualmente, pues se requieren temperaturas extremadamente altas en comparación al vidrio, sin contar la conservación o reestructura necesaria a nivel estructural de los cristales.
Listo, ahora ya sabemos como diferenciar el vidrio del cristal. La próxima vez que alguien trate de venderte una botella de vidrio y te diga que es cristal, sabrás la diferencia.
Tipos de Cristales
Los tipos de cristales se clasifican según su estructura funcional resultado de su proceso de elaboración.
Sólidos: Se considera que todo material que se encuentra en estado sólido ha sido expuesto a un proceso de cristalización, la organización de sus componentes a un fenómeno estructural bajo una secuencia repetitiva sin variaciones irregulares, que van desde la agregación de pequeños cristales o policristalinos (agregado de pequeños cristales) como el hielo, rocas de alta concentración, el hormigón, huesos, metales e incluso los huesos.
Pero esta apreciación no se limita a grandes a escalas sino también a estructuras de menor tamaño como sal, azúcar, piedras preciosas y la mayoría de los minerales, los cuales algunos son usados en la tecnología como el cuarzo de los osciladores o los semiconductores de los dispositivos electrónicos.
Líquidos: Pueden existir cadenas estructurales consistentes en cuerpos líquidos, estas se consideran amorfas, su alcance se logra por medio de un desarrollo incompleto del estado cristalino de solidificación. En la actualidad su uso más común es mediante la colocación de dos láminas de vidrio metalizado la cuales cargan en su interior con una fina película del cristal mesomórfico en las pantallas display de los dispositivos electrónicos, las pantallas LCD, por ejemplo.
Iónicos: Tienen dos características importantes: están formados de enlaces cargados, los aniones y cationes son de distintos tamaños. Son duros y a la vez quebradizos. La fuerza que los mantiene unidos es la electroestática.
Covalentes: Los átomos se mantienen unidos en una red tridimensional únicamente por enlaces covalentes. El grafito (forma más estable del carbono) y el diamante son buenos ejemplos de cristales covalentes.
Moleculares: Los puntos reticulares de un cristal molecular están ocupados por moléculas que se mantienen unidas por la fuerza de Van Der Waals y/o enlaces de hidrógeno. EL dióxido de azufre sólido y el hielo son buenos ejemplos de cristales moleculares. Debido la dependencia estructural tan frágil de estos cristales son propensos a ser quebradizos y la mayoría se funde a temperaturas menores de los 100 grados centígrados.
Metálicos: Son de simple composición pues los puntos reticulares están ocupados por átomos del mismo metal, su estructura suele ser cubica centrada en el cuerpo o las caras; también pueden ser hexagonales de empaquetamiento compacto, por lo que suelen ser densos. Sus propiedades varían de acuerdo a la especie y van desde blandos a duros, manteniendo características de optima conducción térmica y eléctrica.